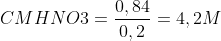nNO= 0,18 (mol)
Gọi số mol của Al và Mg lần lượt là x và y (x; y>0)
QT nhường e: QT Nhận e:
Al---> Al3+ +3e. N5+ +3e----> N2+
Zn---> Zn2+ +2e
BT e: 3nAl + 2nMg= 3nNO---> 3x+2y= 0,54
\(\left\{\begin{matrix} & & 3x+2y=0,54\\ & & 27x+24y= 5,58 \end{matrix}\right.\)
----> \(\left\{\begin{matrix} & & x=0,1 \\ & & y=0,12 \end{matrix}\right.\)
--> nAl=0,1 (mol) -->mAl= 0,1. 27= 2,7 (g)
nMg= 0,12 (mol)--> mMg= 0,12.24= 2,88(g)
b) Dung dịch A có chứa HNO3 dư
Xét phản ứng của Zn với HNO3 (dung dịch A)
4Zn + 10HNO3----> 4Zn(NO3)2 + N2O + 5H2O
0,04------>0,1 0,01 mol)
dung dịch A gồm:

BT N: nHNO3 (bđ) = 3nAl(NO3)3 + 2nMg(NO3)2 + nHNO3 (dư) + nNO+ 2nN2O
->nHNO3(bđ)=3.0,1+2.0,12+0,1+0,18+2.0,01
= 0,84 (mol)