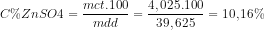a)
Khối lượng của sắt (II) sunfat
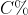 FeSO4
FeSO4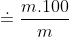
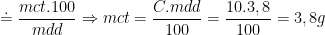
Số mol của sắt (II) sunfat
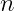
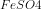
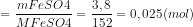
Pt : Zn + FeSO4 → ZnSO4 + Fe||
1 1 1 1
0,025 0,025 0,025 0,025
a) Số mol của kẽm
nZn = 0,025.11=0,025(mol)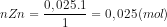
Khối lượng của kẽm
mZn = nZn . MZn = 0,025 . 65
= 1,625 (g)
b) Số mol của sắt
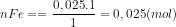
Khối lượng của sắt
mFe= nFe . MFe = 0,025 . 56 = 1,4 (g)
c) Số mol kẽm sunfat
nZnSO4 =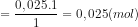
Khối lượng của kẽm sunfat
mZnSO4 = nZnSO4 . MZnSO4
= 0,025 . 161
= 4,025 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mZn + mFeSO4
v = 1,625 + 38= 39,625 (g)
Nồng độ phần trăm của kẽm sunfat