Bảo toàn H có nH2O = naxit nH2O = naxit = 0,32 mol.
Bảo toàn O có:
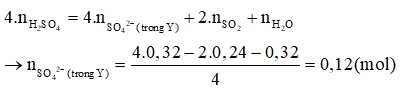
Cho NaOH phản ứng hết với Y, sau phản ứng dung dịch thu được chứa: Na+Na+: 0,25 mol; SO2−4SO42-: 0,12 mol; AlO2−O2- x mol.
Bảo toàn điện tích → x = 0,25 – 2.0,12 = 0,01 (mol)
nOH−(trong↓) = nOH− (ban đầu)nOH-trong↓ = nOH- ban đầu– 4.nAlO2−O2- = 0,25 – 4.0,01 = 0,21 (mol)
mKL (trong ↓)= m ⏐↓− mOH−(trong ↓)mKL trong ↓= m ↓- mOH-trong ↓ = 7,63 – 0,21.17 = 4,06 gam.
Bảo toàn S có:
nS (trong FeS) + nS (trong axit)nS trong FeS + nS trong axit = nS (trong không khí)+ nS (trong SO2−4ở Y )nS trong không khí+ nS trong SO42-ở Y
→ nS (trong FeS)nS trong FeS = 0,24 + 0,12 – 0,32 = 0,04 mol
→ m = mKL (trong ↓)mKL trong ↓ + mS (trong FeS)mS trong FeS + mAl (trong AlO2−)mAl trong AlO2- = 4,06 + 0,04.32 + 0,01.27 = 5,61 gam.